非金属单质燃烧_非金属单质燃烧时火焰有颜色吗
1.为什么氧气支持燃烧
2.非金属单质的化学通性
3.铁与非金属单质反应:(1)Fe在纯O2中燃烧:化学方程式:______;(2)Fe与S的反应:化学方程式:_______
4.燃烧的产物有哪些
5.非金属元素R,其单质4,8g在氧气中充分燃烧生成二氧化R9,6g,在R原子中,核内质子数等于中子数,则R的元...
6.化学的所有反应物公式有哪些
7.硫磺燃烧火焰温度
1、温度不够,由于发动机温度不够,喷入气缸内的燃油与空气形成的混和气,一部分不能燃烧,排气管冒白烟。因此,在机车发动后,应注意水箱的保温,用中油门运转,使机车温度达到50度以上时,在逐渐增大负荷。
2、柴油中有水,柴油中有水,直接影响混和气的正常燃烧,冒白烟。此时,应放出沉淀油,排出积水,必要时更换柴油。
3、如果排气管出现继续冒白烟可能是个别缸的缸盖、缸垫部位损坏进水,应拆下检查,更换损坏的缸盖、缸垫。此外,进气门关闭不严,也会出现白烟,应予检查和修复。
为什么氧气支持燃烧
在常温时:4Na+O2=2Na2O (白色粉末)
在点燃时:2Na+O2=Na2O2 (淡**粉末)
2Na+Cl2=2NaCl (放出大量热,生成大量白烟)
2Na+S=Na2S(硫化钠)(钠与硫化合时研磨会发生爆炸)
2Na+Br2=2NaBr(溴化钠)(溴化钠可以用作)
2Na+H2=高温=2NaH
非金属单质的化学通性
燃烧是金属和非金属单质及某些化合物和氧气的反应称为燃烧。
其条件是: 1.可燃物. 2.氧气(氧化反应的必需品). 3.温度达到燃点.(此燃点和可燃物有关,不同的可燃物对应不同的然点。)燃烧是氧化反应,氧原子容易得到两个电子从而成为8电子稳定结构,具有较强的非金属性,形成的O2单质在化学反应中表现为氧化性,易燃烧,所以支持燃烧。
铁与非金属单质反应:(1)Fe在纯O2中燃烧:化学方程式:______;(2)Fe与S的反应:化学方程式:_______
1.与金属反应:生成无氧酸盐或其他AB型化合物
S+2Na==Na2S(爆炸)
Cl2+Na=点燃=NaCl(剧烈燃烧)
F2+2K===2KF(常温下激烈燃烧)
O2+Cu==加热==CuO
注意:并不是任意一个非金属都能和任意一个金属反应,
这里要求它们至少其中之一要活泼些。
比如:金属Au就不能和O2反应,因为Au很不活泼(真金不怕火炼)。
而Au在微热的条件下就能在F2中燃烧生成AuF3。
2.与H2反应:除了B等少数非金属不与H2化合
F2+H2=暗处=2HF(爆炸)
Cl2+H2==光照==2HCl(爆炸)
Br2+H2==500度==2HBr(反应较慢)
I2+H2==加热,催化剂==2HI(可逆反应)
O2+2H2==点燃==2H2O(激烈燃烧或爆炸)
O3+3H2===零下78度===3H2O(爆炸)
S+H2==300度==H2S(较顺利,但H2S会同时少量分解)
C+2H2==高温==CH4(反应困难)
Si+2H2==高温==SiH4(相当困难)
2P+3H2==高温===2PH3(反应困难,可逆)
3.某些很活泼的非金属还会和别的非金属反应:如O2,F2,Cl2,S等,这几个非金属单质的的电离能力很强,会和得到别的非金属失去的电子而使之氧化,从而显负价。
O2+S==点燃==SO2(O显负-2价)
Cl2+S==加热==SCl2(Cl显-1价)
F2+S===6(F显-1价)
5S+2P==加热==P2S5(S显-1价)
总之的电子能力强的显负价,失电子能力强的显正价!
4.除O2外的大多数非金属单质可以和碱反应:
2F2+2NaOH(2%)===2NaF+OF2+H2O
Cl2+2NaOH==NaCl+NaClO+H2O
3Br2+6KOH==5KBr+KBrO3+3H2O
3S+6NaOH=加热=2Na2S+Na2SO3+3H20
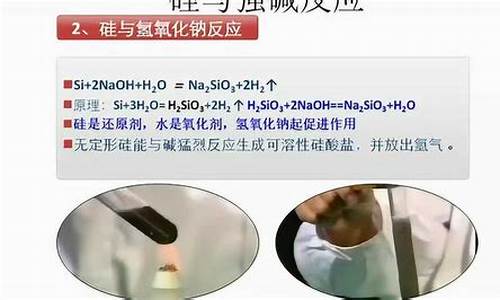
Si+2NaOH+H2O=加热=Na2SiO3+2H2
燃烧的产物有哪些
(1)Fe在纯O?中燃烧生成四氧化三铁,反应的方程式为3Fe+2O?==Fe?O?(条件为点燃)。
(2)S氧化性较弱,Fe与S的反应生成FeS,方程式为Fe+S==FeS(条件为加热)。
(3)氯气氧化性较强,Fe与Cl?点燃条件下生成氯化铁,发生反应为2Fe+3Cl?==2FeCl?(条件为点燃)。
(4)I?氧化性较弱,Fe与I?的反应生成FeI?,方程式为Fe+I?=FeI?。
扩展资料:
铁的原子序数26,铁单质化学式:Fe。纯铁是白色或者银白色的,有金属光泽。熔点1538℃、沸点2750℃,能溶于强酸和中强酸,不溶于水。铁有0价、+2价、+3价和+6价,其中+2价和+3价较常见,+6价少见。
铁在生活中分布较广,占地壳含量的4.75%,仅次于氧、硅、铝,位居地壳含量第四。纯铁是柔韧而延展性较好的银白色金属,用于制发电机和电动机的铁芯,铁及其化合物还用于制磁铁、药物、墨水、颜料、磨料等,是工业上所说的“黑色金属”之一。
铁易溶于稀的无机酸中,生成二价铁盐,并放出氢气。在常温下遇浓硫酸或浓硝酸时,表面生成一层氧化物保护膜,使铁“钝化”,故可用铁制品盛装冷的浓硫酸或冷的浓硝酸。在加热时,铁可以与浓硫酸或浓硝酸反应,生成+3价的铁盐,同时生成SO?或NO?。
百度百科-铁
百度百科-硫
百度百科-氯气
非金属元素R,其单质4,8g在氧气中充分燃烧生成二氧化R9,6g,在R原子中,核内质子数等于中子数,则R的元...
1、部分非金属单质,如碳、硫、磷、硅等;
2、大部分金属单质,如钠、镁、钾、锂等;
3、部分气态氢化物,如H2S、CH4等;
4、少量氧化物,如CO;
5、绝大多数有机物,如甲醇、丙酮、油脂等。
化学的所有反应物公式有哪些
R + O2=RO2 质量守恒,燃烧时用去R 9.6-4.8=4.8g
x 32
4.8g 4.8g 4.8x=4.8*32 x=32 硫 最高价:+6
硫磺燃烧火焰温度
化学的所有反应物公式有哪些
与非金属单质反应
1、碳在氧气中充分燃烧:C+ O2 点燃 CO2
现象:燃烧旺盛、发白光、放热、生成的气体能使石灰水变浑浊
2、碳在氧气中不充分燃烧:C+ O2 点燃 2CO
氧气不充足时生成一氧化碳.燃烧、放热.生成有毒的气体CO
3、硫在氧气中燃烧:S+ O2 点燃 SO2
现象:产生明亮的蓝紫色火焰、放热、生成的气体有刺激味气体(硫在空气中燃烧是淡蓝色火焰)
4、红磷在氧气中燃烧:4P + 5O2点燃 2P2O5
现象:剧烈燃烧、放热、有浓厚的白烟生成.
5、氢气在空气中燃烧:2H2 +O2 点燃 2H2O
现象:燃烧、放热、淡蓝色火焰,干燥的烧杯壁有水雾出现
与金属单质的反应
6、镁条子空气中燃烧:2Mg +O2 点燃 2MgO
现象:剧烈燃烧,发出耀眼的白光,放热,生成白色固体
7、铁丝在氧气中燃烧:3Fe+2 O2 点燃 Fe3O4
现象:剧烈燃烧、火星四射、放出大量的热、生成黑色固体
注意:①做此实验时,瓶底要放少量细沙或水,防止生成的高温的熔化物溅落炸裂瓶底.
②铁在空气中不能燃烧,所以实验时,铁丝一端要系一根火柴,待火柴即将燃尽时放入氧气瓶中, 用火柴在氧气中燃烧的热量引燃铁丝.
8、氧气通过灼热的铜网:2Cu+ O2 加热 2CuO 现象:红色金属铜变为黑色固体
9、铝箔在氧气中燃烧:4Al + 3O2 点燃 2Al2O3
现象:剧烈燃烧、放热、耀眼的白光, 生成白色固体
10、密闭容器中加热金属汞:2Hg+O2 加热 2HgO
现象:银白色的液体变成桔红色粉末,同时容器里的空气的体积差不多减少了1/5.(拉瓦锡著名的测定空气成分的实验)
248至261摄氏度。
硫磺属易燃物,固体硫磺燃烧温度在248至261摄氏度,粉状硫磺燃烧温度为190摄氏度,液硫自燃温度为230摄氏度。硫磺燃烧需要大量氧,因此纯硫磺在空气中燃烧时火焰较短。
硫磺,别名硫,是一种非金属单质,化学式为S,为淡**脆性结晶或粉末,有特殊臭味,不溶于水,微溶于乙醇、,易溶于二硫化碳。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。












