金属单质与酸反应吗_金属单质与酸反应
1.金属与酸的反应
2.金属单质与酸反应,生成物中,金属单质的化合价
3.酸能与金属活动性顺序表中氢前面的金属发生什么反应
4.性强弱为什么要单质与酸与水反应来判
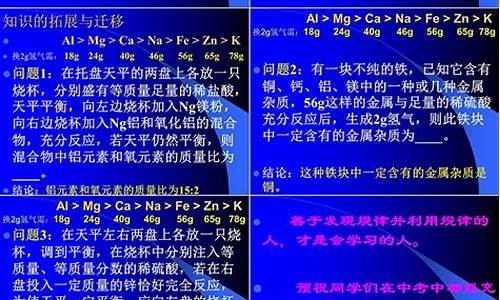
(1)金属单质 + 酸 -------- 盐 + 氢气 (置换反应)
29. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑
30. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑
31. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑
32. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑
33. 锌和稀盐酸Zn + 2HCl === ZnCl2 + H2↑
34. 铁和稀盐酸Fe + 2HCl === FeCl2 + H2↑
35. 镁和稀盐酸Mg+ 2HCl === MgCl2 + H2↑
36. 铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑
(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐
37. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu
38. 锌和硫酸铜溶液反应:Zn + CuSO4 = ZnSO4 + Cu
39. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 = Cu(NO3)2 + Hg
(3)碱性氧化物 +酸 -------- 盐 + 水
40. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl = 2FeCl3 + 3H2O
41. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O
42. 氧化铜和稀盐酸反应:CuO + 2HCl = CuCl2 + H2O
43. 氧化铜和稀硫酸反应:CuO + H2SO4 = CuSO4 + H2O
44. 氧化镁和稀硫酸反应:MgO + H2SO4 = MgSO4 + H2O
45. 氧化钙和稀盐酸反应:CaO + 2HCl = CaCl2 + H2O
(4) 酸性氧化物 +碱 -------- 盐 + 水
46.苛性钠暴露在空气中变质:2NaOH + CO2 = Na2CO3 + H2O
47.苛性钠吸收二氧化硫气体:2NaOH + SO2 = Na2SO3 + H2O
48.氢氧化钠吸收三氧化硫气体:2NaOH + SO3 = Na2SO4 + H2O
49.熟石灰放在空气中变质:Ca(OH)2 + CO2 = CaCO3 ↓+ H2O
50.熟石灰吸收二氧化硫:Ca(OH)2 + SO2 = CaSO3 ↓+ H2O
(5)酸 + 碱 -------- 盐 + 水
51.盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O
52.盐酸和氢氧化钾反应:HCl + KOH ==== KCl +H2O
53.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 + 2H2O
54.盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O
55.盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 + 3H2O
56.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O
57.硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O
58.硫酸和氢氧化钾反应:H2SO4 + 2KOH ==== K2SO4 + 2H2O
59.硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ==== CuSO4 + 2H2O
60.硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O
61.硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O
(6)酸 + 盐 -------- 另一种酸 + 另一种盐
62.碳酸钙与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
63.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑
64.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2 + H2O + CO2↑
65.盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO3
66.硫酸和碳酸钠反应:Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2↑
67.硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ==== BaSO4 ↓+ 2HCl
(7)碱 + 盐 -------- 另一种碱 + 另一种盐
68.氢氧化钠与硫酸铜:2NaOH + CuSO4 ==== Cu(OH)2↓ + Na2SO4
69.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl
70.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl
71.氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl
72.氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH
(8)盐 + 盐 ----- 两种新盐
73.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO3
74.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl
金属与酸的反应
金属单质 + 酸 ---- 盐 + 氢气 (置换反应)
1、锌和稀硫酸反应:Zn + H2SO4 === ZnSO4 + H2↑
2、镁和稀硫酸反应:Mg + H2SO4 === MgSO4 + H2↑
3、铝和稀硫酸反应:2Al + 3H2SO4 === Al2(SO4)3 + 3H2↑
4、锌和稀盐酸反应:Zn + 2HCl === ZnCl2 + H2↑
5、镁和稀盐酸反应:Mg+ 2HCl === MgCl2 + H2↑
6、铝和稀盐酸反应:2Al + 6HCl === 2AlCl3 + 3H2↑
现象:有气泡产生.
7、铁和稀盐酸反应:Fe + 2HCl === FeCl2 + H2↑
8、铁和稀硫酸反应:Fe + H2SO4 === FeSO4 + H2↑
现象:有气泡产生,溶液由无色变成浅绿色.
复分解反应:
(1)碱性氧化物+酸→盐+H2O
Fe2O3+6HCl==2FeCl3+3H2O Fe2O3+3H2SO4==Fe2(SO4)3+3H2O
CuO+H2SO4==CuSO4+H2O ZnO+2HNO3==Zn(NO3)3+H2O
(2)碱+酸→盐+H2O
Cu(OH)2+2HCl==CuCl2+2H2O Cu(OH)2+H2SO4==CuSO4+2H2O
NaOH+HCl==NaCl+H2O 2NaOH+H2SO4==Na2SO4+2H2O
NaOH+HNO3==NaNO3+H2O Mg(OH)2+2HNO3==Mg(NO3)2+2H2O
Ba(OH)2+H2SO4==BaSO4↓+2H2O
(3)酸+盐→新盐+新酸
CaCO3+2HCl==CaCl2+H2O+CO2↑ Na2CO3+2HCl==2NaCl+H2O+CO2↑
HCl+AgNO3==AgCl↓+HNO3 H2SO4+BaCl2==BaSO4↓+2HCl
Ba(NO3)2+H2SO4==BaSO4↓+2HNO3
NaHCO3+HCl==NaCl+H2O+CO2↑
(4)盐1+盐2→新盐1+新盐2
KCl+AgNO3==AgCl↓+KNO3 NaCl+AgNO3==AgCl↓+NaNO3
Na2SO4+BaCl2==BaSO4↓+2NaCl BaCl2+2AgNO3==2AgCl↓+Ba(NO3)2
(5)盐+碱→新盐+新碱
CuSO4+2NaOH==Cu(OH)2↓+Na2SO4 FeCl3+3NaOH==Fe(OH)3↓+3NaCl
Ca(OH)2+Na2CO3==CaCO3↓+2NaOH NaOH+NH4Cl==NaCl+NH3↑+H2O
酸性氧化物 +碱 -------- 盐 + 水
1、二氧化碳通入澄清石灰水:CO2 +Ca(OH)2 ==CaCO3↓+ H20
现象:澄清石灰水变浑浊.(用澄清石灰水可以检验CO2,也可以用CO2检验石灰水)
2、氢氧化钙和二氧化硫反应:SO2 +Ca(OH)2 ==CaSO3+ H20
3、氢氧化钙和三氧化硫反应:SO3 +Ca(OH)2 ==CaSO4+ H20
4、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH + CO2 ==== Na2CO3 + H2O
5、氢氧化钠和二氧化硫反应(除去二氧化硫):2NaOH + SO2 ==== Na2SO3 + H2O
6、氢氧化钠和三氧化硫反应(除去三氧化硫):2NaOH + SO3 ==== Na2SO4 + H2O
金属单质与酸反应,生成物中,金属单质的化合价
金属和酸的反应指的是酸与金属发生置换反应。不是所有金属都与酸反应。
只有金属活动顺序中位于氢前面的金属才与酸反应。 金属单质 + 酸 -------- 盐 + 氢气 (置换反应),金属单质 + 盐(溶液) ---另一种金属 + 另一种盐,金属氧化物+木炭或氢气→金属+二氧化碳或水。
当你把一片铁或锌放入酸液时,它们会很快的发生反应:又是放热,又是冒泡,后来这片金属就慢慢地消失了。这往往使人们以为,凡是金属都能跟酸起反应。其实,并不都是如此。有的金属跟一种酸能起反应,跟另一种酸就不起反应;而每种酸也不一定跟各种金属都能起反应。
酸能与金属活动性顺序表中氢前面的金属发生什么反应
其实你是初三的学生吧?那就不说那么复杂了
方程式为 2 M(金属) + 2n H+ ==== 2 M n+(n个正电荷)+ n H2
质量:2M(该金属相对原子质量) 2n
投入:m x
(那个X不知道为什么移不到2n下面去)
有2M/m=2n/x
化简得:x=mn/M
即 放出氢气的质量=金属元素在生成物中化合价×金属质量÷该金属相对原子质量
这只是化学方程式啊!
性强弱为什么要单质与酸与水反应来判
发生置换反应。
氢前面的可以和酸反应生成氢气,而氢后面的基本不和酸反应就算反应也不生成氢气.
金属单质 + 酸 —— 盐 + 氢气
部分化学方程式:
1、锌和稀硫酸反应:Zn + H?SO? = ZnSO? + H?↑
2、锌和稀盐酸反应:Zn + 2HCl = ZnCl? + H?↑
3、铝和稀硫酸反应:2Al + 3H?SO? = Al?(SO?)? + 3H?↑
4、铝和稀盐酸反应:2Al + 6HCl = 2AlCl? + 3H?↑
5、镁和稀盐酸反应:Mg+ 2HCl = MgCl? + H?↑
6、镁和稀硫酸反应:Mg + H?SO? = MgSO? + H?↑
1~6的现象:有气泡产生。
7、铁和稀盐酸反应:Fe + 2HCl = FeCl? + H?↑
8、铁和稀硫酸反应:Fe + H?SO? = FeSO? + H?↑
7~8铁参加的置换反应显+2价,7~8的现象:有气泡产生,溶液由无色变成浅绿色。
注意:浓盐酸在加热时也能与铜(不太活泼的金属)反应,这是因为Cl和Cu形成了较稳定的配离子[CuCl4],使Cu=Cu + e的平衡向右移动:2Cu + 8HCl(浓)== 2H3[CuCl4] + H2↑[2]
首先一点,元素的金属性是指元素的原子失电子的能力.
金属性越强,则越容易失去电子.金属性的强弱就是失去电子能力的难易程度.把这点概念先搞清楚.
金属单质与酸反应的本质是:一个金属R,与酸释放出来的H+反应,R失去电子,H+得到电子.
OK,现在得电子的物质是相同的,都是H+,那只需比较金属R失电子的难以程度即可比较金属性的强弱.
在酸溶液中,H+的浓度比较大,通过金属反应时放氢气的速率来比较.
但是有的金属性非常强的金属,就很难通过和酸反应来比较了.凭眼睛的观察是感觉不出来放氢气的差异的.所以就要通过跟水的反应来比较.水会微弱电离,产生极少量的H+,你可以把水视为一种弱酸.一个金属能跟水反应,一个不能跟水反应,两者失电子能力一目了然.
跟水反应时的剧烈程度也能比较出金属性强弱,越剧烈者,越易失电子,则金属性越强.反之亦然.
跟水反应的条件也可以比较,钠与水直接反应,镁与水反应需加热.条件越简单,金属性越强,条件越苛刻,则电子越难失去,金属性亦弱.
其实金属性的强弱比较,类似于比较非金属性的强弱,相互印证对比,相信对你理解这样的问题有更大的帮助.想想卤素跟氢气反应的难以程度.通过反应条件来比较元素的性质是常用的方法.
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。