氯气和金属单质反应_氯气和金属单质反应生成什么价态
1.氯气与足量金属反应
2.硫(氯气)与金属反应规律
3.铜和氯气反应
4.求氯气与单质的反应现象和化学式
5.高中化学+氯气所有反应
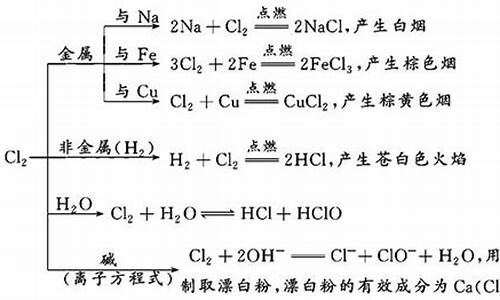
铝和氯气反应如下:
铝和氯气反应是一种重要的化学反应,通常在常温常压下进行。这个反应中,铝原子与氯气分子中的氯原子发生键合,生成氯化铝。这个反应是非常重要的,因为它在很多化学工业过程中都得到了应用,例如制造塑料、农药、漂白剂等。
在标准状态下,这是一个放热反应,反应过程中会释放出大量的热能。这个反应也是路易斯酸碱反应的一种,其中铝原子作为路易斯碱,氯气分子作为路易斯酸。
铝和氯气反应非常明显,通常会伴随剧烈的燃烧和发出明亮的白光。在反应过程中,铝原子会失去三个电子,而每个氯原子则会得到一个电子,形成稳定的氯化铝。
这个反应是可逆的,如果改变反应条件,比如增加温度或者改变压力,则可以使得反应向相反方向进行,生成铝和氯气。
氯化铝是一种非常重要的化合物,它在水溶液中是一种强酸,也称为氢氯酸。氯化铝可以用于制造其他化学品,例如聚氯化铝、氯化铝分解涂料等。此外,氯化铝还可以用于电镀、造纸、纺织等工业领域。
除了铝和氯气反应本身,这个反应还有一些重要的。首先,这个反应可以用于制备高纯度的铝单质。通过将铝粉和氯气反应,可以制备出高纯度的氯化铝,然后再通过电解还原的方法将其还原为高纯度的铝单质。
其次,这个反应还可以用于制备其他金属氯化物。例如,将铝和氯化铁反应可以制备出氯化铁。此外,铝和氯气反应还可以用于制备其他含氯化合物,例如次氯酸、氯代烃等。
此外,铝和氯气的反应还可以用于制备其他金属氯化物。例如,将铝和氯化铁反应可以制备出氯化铁。氯化铁是一种重要的工业原料,可以用于制造染料、农药、医药等。
此外,铝和氯化铜也可以反应,制备出氯化铜。氯化铜是一种常见的催化剂和电极材料,可以用于制造电池、电解槽等。
另外,铝和氯气的反应还可以用于制备其他含氯化合物。例如,将铝和次氯酸反应可以制备出次氯酸。次氯酸是一种强氧化剂,可以用于漂白、消毒等应用。此外,将铝和氯气反应还可以制备出氯代烃。氯代烃是一种重要的有机化工原料,可以用于制造农药、医药、香料等。
总之,铝和氯气反应是一种非常重要的化学反应,它在化学工业中得到了广泛的应用。通过了解这个反应的原理和,我们可以更好地理解化学反应的本质和应用,同时也为相关领域的研究和应用提供一些参考和启示。
氯气与足量金属反应
和金属单质反应:1、和钠反应生成氯化钠; 2、和Fe反应生成氯化铁 3、和铜反应生成氯化铜;和非金属单质反应:1、和氢气反应生成氯化氢 2、和硫单质反应生成硫化氢 3、和磷单质反应生成三氯化磷和五氯化磷
硫(氯气)与金属反应规律
首先明确这些反应是氧化还原反应就好办了!
0.15mol的Cl2中有0.3mol的Cl原子,反应后变为Clˉ,关系式如下:
Cl+eˉ=Clˉ
1~~1
0.3~0.3
所以全部反应需要0.3mol的电子转移,而这里有0.1mol的金属单质,所以该金属和Cl2反应后的化合物中金属元素为0.3/0.1=+3价
这里就可以排除AB了!~
硫那个也一样,列出还原反应的关系式:
S+2eˉ=(S)2ˉ
1~2
0.1~0.2
所以全部反应需要0.2mol的电子转移,,而这里有0.1mol的金属单质,所以该金属和S反应后的化合物中金属元素为0.2/0.1=+2价
到这里就没问题了,因为Al元素没见过+2价,所以答案是铁,选D。这里只有铁有+3和+2价!
铜和氯气反应
由于硫单质的氧化性弱,氯单质的氧化性强,所以在与金属反应的时候特点不一样。氯气与金属反应都是将金属氧化为最高价,比如与铁反应,生成氯化铁,不会生成氯化亚铁。而硫单质与铁反应只能生成硫化亚铁。与硫单质类似的还有碘单质。
求氯气与单质的反应现象和化学式
铜和氯气反应如下可供参考:
一、反应情况
Cu+Cl2==点燃==CuCl2,生成大量红棕色烟雾。
二、铜
1、铜(Cuprum)是一种金属元素,也是一种过渡元素,化学符号Cu,英文copper,原子序数29。纯铜是柔软的金属,表面刚切开时为红橙色带金属光泽,单质呈紫红色。延展性好,导热性和导电性高,因此在电缆和电气、电子元件是最常用的材料。
2、也可用作建筑材料,可以组成众多种合金。铜合金机械性能优异,电阻率很低,其中最重要的数青铜和黄铜。此外,铜也是耐用的金属,可以多次回收而无损其机械性能。铜是人类最早使用的金属之一。
3、早在史前时代,人们就开始掘露天铜矿,并用获取的铜制造武器、工具和其他器皿,铜的使用对早期人类文明的进步影响深远。铜是一种存在于地壳和海洋中的金属。
4、铜在地壳中的含量约为0.01%,在个别铜矿床中,铜的含量可以达到3%~5%。自然界中的铜,多数以化合物即铜矿石存在。
三、氯气
1、氯气(chlorine)是氯元素形成的一种单质,化学式Cl2。常温常压下为黄绿色,有强烈刺激性气味的剧毒气体,具有窒息性,密度比空气大。熔点-101.00℃,沸点-34℃。可溶于水和碱溶液,易溶于有机溶剂(如四氯化碳),难溶于饱和食盐水。
2、易压缩,可液化为黄绿色的油状液氯。氯气中混合体积分数为5%以上的氢气时遇强光可能会有爆炸的危险。氯气具有毒性,主要通过呼吸道侵入人体并溶解在黏膜所含的水分里,会对上呼吸道黏膜造成损害。
高中化学+氯气所有反应
1、现象:钠在氯气里剧烈燃烧,产生大量的白烟,放热。2Na+Cl2=点燃=2NaCl
2、现象:红热的铜丝在氯气里剧烈燃烧,瓶里充满棕**的烟,加少量水后,溶液呈蓝绿色。Cu+Cl2=点燃=CuCl2
3、现象:铁丝在氯气里剧烈燃烧,瓶里充满棕红色烟,加少量水后,溶液呈**。 2Fe+3Cl2=点燃=2FeCl3与金属反应
4、与氢气的反应
H2+Cl2=点燃=2HCl(工业制盐酸方法,工业先电解饱和食盐水,生成的氢气和氯气燃烧生成氯化氢气体)现象:H2在Cl2中安静地燃烧,发出苍白色火焰,瓶口处出现白雾。
H2+Cl2=光照=2HCl 现象:见光爆炸,有白雾产生。
5、与磷的反应
2P+3Cl2(少量)=点燃=2PCl3(液体农药,雾)
2P+5Cl2(过量)=点燃=2PCl5(固体农药,烟) 现象:产生白色烟雾
(1)、氯气与大多数金属反应。(与铁、铜等变价金属反应时,生成高价氯化物) (2)、氯气与磷反应3Cl2+2P==2PCl3(点燃)PCl3+Cl2==PCl5(白色烟雾) (3)、氯气与氢气反应(纯净氢气在氯气中安静燃烧发出苍白色火焰;混合气光照爆炸;卤素单质的活泼程度比较) (4)、氯气与水反应:氯水的多重性质(Cl2的强氧化性、次氯酸的强氧化性、次氯酸的不稳定性、 盐酸的酸性、次氯酸的酸性) (5)、氯气与氢氧化钠溶液反应(用氢氧化钠溶液吸收残余氯气) (6)、氯气与氢氧化钙反应 (7)、氯气与溴化钠溶液反应 (8)、氯气与碘化钾溶液反应 (9)、氯气与甲烷取代反应 (10)、氯气与乙烯的反应 (11)、氯气与氯化亚铁溶液反应 (12)、氯气与硫化氢溶液反应 (13)、氯气与二氧化硫溶液反应 (14)、氯气的检验方法——淀粉碘化钾试纸
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。