黑色非金属单质_黑色非金属单质有哪些
1.高中化学关于金属与非金属固体颜色总结
2.什么决定单质的颜色
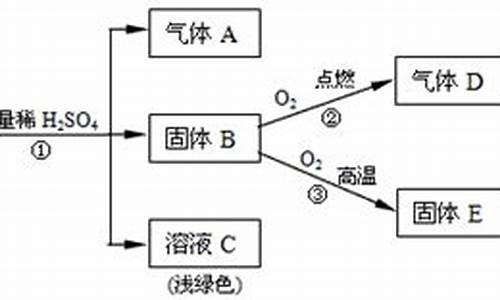
3.A、X、6、七是中学常见的单质和化合物.它们在一定条件下能发生如下转化,转化中的部分产物已省略.(二
无机推断题常见突破点归纳
1. 特殊颜色
(1)火焰颜色
苍白色:H2在Cl2中燃烧
蓝色:CO在空气中燃烧
淡蓝色:H2S、CH4、H2在空气中燃烧
焰色反应:Na+(**)、K+(紫色)
(2)有色溶液
Fe2+:浅绿色
Fe3+:**
Cu2+:蓝色
MnO4-:紫红色
(3)有色固体
红色:Cu、Cu2O、Fe2O3
红褐色:Fe(OH)3
绿色:Cu2(OH)2CO3、FeSO4.7H2O
蓝色:Cu(OH)2、CuSO4.5H2O
黑色:CuO、FeO、FeS、CuS、MnO2、PbS、炭黑
浅**:S、Na2O2、AgBr
**:AgI、Ag3PO4
白色:Fe(OH)2、CaCO3、BaSO4、AgCl、BaSO3
有色气体:
黄绿色:Cl2
红棕色:NO2
1)溶于水显碱性的气体只有NH3
(2)在空气中迅速由无色变为红棕色的气体只有NO
(3)能与SO2等气体或其水溶液作用析出浅**固体的只有H2S(包括与Cl2、O2、NO2等氧化性较强的气体作用均有此现象)。
(4)在一定条件下能漂白有色物质的淡**固体只有Na2O2
(5)在空气中能自燃的固体物质只有白磷
(6)遇SCN-显红色的只有Fe3+
(7)常见的可溶于NaOH溶液的白色沉淀有Al(OH)3和Zn(OH)2,可溶于NaOH溶液的金属氧化物有Al2O3和ZnO。
(8)可溶于氢氟酸的酸性氧化物只有SiO2
(9)能与盐酸作用产生无色无味的气体,且通入澄清石灰水中能产生白色沉淀的,只有含(CO3)2-或(HCO3)2-的物质。
(10)能与盐酸作用产生有刺激性气味的无色气体,且通入品红溶液中能使之褪色,加热又复原的只有含(SO3)2-或(HSO3)2-的物质。
(11)能与浓H2SO4、铜片共热产生红棕色气体的晶体只有硝酸盐。
(12)通入CO2能产生白色胶状沉淀且不溶于任何酸的溶液中一定含有(SiO3)2-。
(13)需要控制在170℃才能生成的气体只有C2H4。
(14)能与新制悬浊液混Cu(OH)2合加热生成砖红色沉淀的酸性物质只有甲酸。
(15)不溶于水又不溶于稀盐酸或稀硝酸的化合物有:BaSO4(白色)、AgCl(白色)、CuS(黑色)、PbS(黑色)等。
(16)有消毒、杀菌和漂白作用的物质有:HClO、H2O2、Na2O2、O3和SO2等。
3. 特征反应
(1)能与强酸反应产生气体的物质:
活泼的金属:Na、Al、Zn等;不稳定的弱酸盐:碳酸盐、碳酸氢盐、硫化物、亚硫酸盐等。
(2)能与强碱或其溶液反应产生气体的物质:
单质:Al、Si;盐类:铵盐、羧酸盐(与碱石灰共热)等。
(3)既能与强酸又能与强碱溶液反应的物质:
金属单质:Al、Zn等;氧化物:Al2O3、ZnO等;氢氧化物:Al(OH)3、Zn(OH)2等;弱酸的铵盐:NH4HCO3、(NH4)2CO3、(NH4)2S、(NH4)2SO3等;弱酸的酸式盐:NaHCO3、NaHS、NaHSO3等;氨基酸。
(4)能与水反应产生气体的物质:
活泼的金属单质:Na、K、Mg(加热)、Fe(高温生成Fe3O4)等;非金属单质:F2;金属过氧化物:Na2O2等;金属碳化物:CaC2等;金属氮化物:Mg3N2等。
高中化学关于金属与非金属固体颜色总结
1、 常见物质的颜色:多数气体为无色,多数固体化合物为白色,多数溶液为无色。
2、 一些特殊物质的颜色:
黑色:MnO2、CuO、Fe3O4、C、FeS(硫化亚铁)
蓝色:CuSO4?5H2O、Cu(OH)2、CuCO3、含Cu2+ 溶液、
液态固态O2(淡蓝色)
红色:Cu(亮红色)、Fe2O3(红棕色)、红磷(暗红色)
**:硫磺(单质S)、含Fe3+ 的溶液(棕**)
绿色:FeSO4?7H2O、含Fe2+ 的溶液(浅绿色)、碱式碳酸铜[Cu2(OH)2CO3]
无色气体:N2、CO2、CO、O2、H2、CH4
有色气体:Cl2(黄绿色)、NO2(红棕色)
有刺激性气味的气体:NH3(此气体可使湿润pH试纸变蓝色)、SO2
有臭鸡蛋气味:H2S
3、 常见一些变化的判断:
① 白色沉淀且不溶于稀硝酸或酸的物质有:BaSO4、AgCl(就这两种物质)
② 蓝色沉淀:Cu(OH)2、CuCO3
③ 红褐色沉淀:Fe(OH)3
Fe(OH)2为白色絮状沉淀,但在空气中很快变成灰绿色沉淀,再变成Fe(OH)3红褐色沉淀
④沉淀能溶于酸并且有气体(CO2)放出的:不溶的碳酸盐
⑤沉淀能溶于酸但没气体放出的:不溶的碱
什么决定单质的颜色
白色沉淀:Fe(OH)2,CaCO3,BaSO4,Mg(OH)2,Al(OH)3,PbSO4,AgCl ,ZnS
红褐色沉淀:Fe(OH)3
蓝色沉淀:Cu(OH)2
黑色沉淀:CuS,PbS,FeS,Ag2S,HgS
浅**沉淀:AgBr
**沉淀:AgI
砖红色沉淀:Gu2O
(一)、固体的颜色
1、红色固体:铜,氧化铁
2、绿色固体:碱式碳酸铜
3、蓝色固体:氢氧化铜,硫酸铜晶体
4、紫黑色固体:高锰酸钾 ,碘单质
5、淡**固体:硫磺
6、无色固体:冰,干冰,金刚石
7、银白色固体:银,铁,镁,铝,汞等金属
8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭),氧化亚铁
9、红褐色固体:氢氧化铁 ,氧化铁
10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁
**固体:铬酸钾
(二)、液体的颜色
11、无色液体:水,双氧水
12、蓝色溶液:铜离子溶液 ,蛋白质与双缩尿试剂生成蓝色
13、蓝绿色溶液:亚铁离子溶液
14、棕**溶液:铁离子溶液
15、紫红色溶液:高锰酸钾溶液
16、紫色溶液:石蕊溶液,三价铁离子与苯酚生成紫色络合物
棕红色液体:液溴
**溶液:二氧化氮溶液,溴溶液(随浓度增加变为橙色),碘溶液(浓度增加变为褐色),蛋白质遇浓硝酸为**
红色溶液:硫氰化钾
(三)、气体的颜色
17、红棕色气体:二氧化氮,溴气体
18、黄绿色气体:氯气
19、无色气体:氧气,氮气,氢气,二氧化碳,一氧化氮,一氧化碳,二氧化硫,氯化氢气体等大多数气
淡黄绿色:氟气体
**:
(四),颜色反应
钠 **
钾 紫色(透过蓝色钴玻璃)
铜 绿色
钙 砖红色
锂 紫红色
总结过去所学过的知识,还是自己做更有印象
我在搜集这些知识也复习一遍,谢谢啦!
A、X、6、七是中学常见的单质和化合物.它们在一定条件下能发生如下转化,转化中的部分产物已省略.(二
金属和非金属单质物理性质.
金属单质:记住除Ag**,Cu紫红色,Mn紫色其他是白色(包括Fe,我们老师说的),状态嘛Hg是液态其他都是固态。
非金属单质:气态的都是含“气”字旁的,其他固态含“石”字旁。颜色那就靠自己积累了,eg:cl2黄绿色,S**,C黑色,这就不能具体了。
金属化合物我也告诉你点:
白色:NaOH、Mg(OH)2、Al(OH)3
Zn(OH)2、Fe(OH)2、AgOH
红褐色:Fe(OH)3
蓝色:Cu(OH)2
白色固体:Na2O、MgO、Al2O3、ZnO
淡**粉末:Na2O2
红色固体:Fe2O3、Cu2O、HgO
黑色粉末:FeO、Fe3O4、CuO、Ag2O
Fe,Zn,Al(除Mn,Cu,Ag)等金属单质都是银白色(这是毋庸质疑的),金属单质都是有金属光泽的,有延展性,能导电能导热
①一般说来金属单质具有金属光泽,大多数金属为银白色;非金属单质一般不具有金属光泽,颜色也是多种多样。 ②金属除汞在常温时为液态外,其他金属单质常温时都呈固态;非金属单质在常温时多为气态,也有的呈液态或固态。 ③一般说来,金属的密度较大,熔点较高;而非金属的密度较小,熔点较低。 ④金属大都具有延展性,能够传热、导电;而非金属没有延展性,不能够传热、导电。 必须明确上述各点不同,都是“一般情况”或“大多数情况”,而不是绝对的。实际上金属与非金属之间没有绝对的界限,它们的性质也不是截然分开的。有些非金属具有一些金属的性质,如石墨是非金属,但具有灰黑色的金属光泽,是电的良导体,在化学反应中可做还原剂;又如硅是非金属,但也具有金属光泽,硅既不是导体也不是绝缘体,而是半导体。也有某些金属具有一些非金属的性质,如锑虽然是金属,但它的性质非常脆,灰锑的熔点低、易挥发等,这些都属于非金属的性质。金属 金属元素的原子结构特征是最外层电子数较少,一般为1—3 个,且在化学反应中较易失去,从而使次外层变为最外层,通常达到8 个电子的稳定结构。原子结构的这一特征,决定了金属的性质特点。 物理性质方面:金属有金属光泽、不透明、容易传热、导电,可以被拉成细丝、展成薄片、塑成各种形状。不少金属(游离态及其化合态)在火焰上灼烧时,会使火焰呈现特殊的颜色,根据这种颜色可以判定某种金属或金属离子的存在。如钠呈**、钾呈浅紫色(透过蓝色的钴玻璃观察)、钙呈砖红色、铜呈绿色。金属也具有各自不同的密度、熔点、硬度等。如密度最小的锂Li(只0.534克/厘米3,20℃)、熔点最低的汞Hg 为-38.87℃、而钨的熔点高达3370℃。非金属单质性质:由非金属元素组成的单质。物理性质差别较大,在许多方面与金属相反。(1)在常温下,形态不一。除溴是液态外,有的是气态,如氢、氧、氮等;有的是固态,如碳、磷、硫等。(2)多数没有光泽,颜色也不一致。(3)通常没有延展性,(4)导热性差。除石墨(碳)、晶体硅、碲等少数外,一般是不良导体。(5)密度较小。固态的密度大都在2-5之间,在5以上的只有砷、碲等少数。非金属的化学性质差别也较大。惰性气体难与他种元素化合。非金属倾向于得到电子,容易与金属化合。在常温下,除磷外,都比较稳定。在高温时,大都能与氧化合而成酸性氧化物。有些非金属与金属之间,很难划分界限 非金属单质物理性质: ( a )分子晶体:熔、沸点较低、硬度小。例如: H2、CL2、F2、、硫磺、白磷等。 ( b )原子晶体:熔、沸点较高,硬度大。例如:金刚石、单晶硅等。 Na物理性质:金属钠很软,可以用刀切割。切开外皮后,可以看到钠具有银白色的金属光泽。钠是热和电的良导体。钠的密度是0.g/cm3,比水的密度小,钠的熔点是.81℃,沸点是882.9℃。 铝是银白色的轻金属,较软,密度2.7g/cm3,熔点660.4℃,沸点2467℃,铝和铝的合金具有许多优良的物理性质,得到了非常广泛的应用。铝对光的反射性能良好,反射紫外线比银还强,铝越纯,它的反射能力越好,常用真空镀铝膜的方法来制得高质量的反射镜。真空镀铝膜和多晶硅薄膜结合,就成为便宜轻巧的太阳能电池材料。铝粉能保持银白色的光泽,常用来制作涂料,俗称银粉。纯铝的导电性很好,仅次于银、铜,铝是热的良导体铝有良好的延展性Mg物理性质:银白色的金属,密度1.74克/厘米3,熔点648.8℃。沸点1107℃。化合价+2,电离能7.646电子伏特,是轻金属之一,具有展性,金属镁无磁性,且有良好的热消散性。铁的物理性质物理性质:铁Fe,原子序数26,相对原子质量55.847。是一种光亮的银白色金属。密度7.86克/厘米3。熔点1535℃,沸点2750℃。常见化合价+2和+3,有好的延展性和导热性。也能导电。纯铁既能磁化,又可去磁,且均很迅速。电离能为7.870电子伏特。 铜的物理性质:纯铜呈紫红色,熔点约1083.4℃,沸点2567℃,密度8.92g/cm3,具有良好的延展性。1g纯铜可拉成3000m细铜丝或压延成面积为10m2几乎透明的铜。锌的物理性质:金属锌,化学符号Zn。属化学元素周期表第II族副族元素,是六种基本金属之一。锌是一种白色略带蓝灰色金属,具有金属光泽,在自然界中多以硫化物状态存在。锌的密度为7.2克/立方厘米,熔点为419.5℃,沸点906℃,莫氏硬度为2.5,其六面体晶体结构稳定性极强。锌较软,仅比铅和锡硬,展性比铅小,比铁大;展性比铜和锡小。细粒结晶的锌比粗粒结晶的锌容易锟轧及抽丝。
ZJ
(3)A为氧化性3单质,Z为淡**固体,Z应为Na2O2,X为Na,A为O2,Y为Na2O,Na2O2由钠离子与过氧根离子构成,阴阳离子个数3最简比是3:2,过氧化钠投入到含有少量酚酞3水溶液中,反应生成氢氧化钠与氧气,溶液呈碱性,故溶液变红,由于过氧化钠有强氧化性,使红色又褪去,故现象为:有气泡产生,溶液先变红后再褪色,
故答案为:3:2;有气泡产生,溶液先变红后再褪色;
(2)A既是氧化物又是氢化物,应为H2O,X为黑色非金属单质,则X为C,碳与水蒸气反应生成Y为CO,反应方程式为:C+H2O(g)
| ||
| ? |
故答案为:C+H2O(g)
| ||
| ? |
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。