碱金属单质密度变化规律_碱金属单质密度
1.碱金属的硬度,密度,熔点,状态,颜色,化学性质各是啥?!急急急~~~~
2.碱金属的物理性质
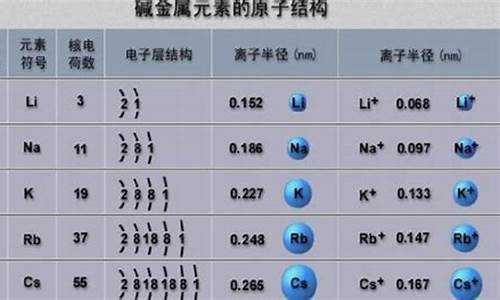
碱金属是指在元素周期表中ⅠA族除氢(H)外的六个金属元素,即锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr)。
锂的密度为0.534g/cm?,熔点为180.5 °C;沸点1342?°C;
钠的密度为0.1g/cm?,熔点为.81 °C,沸点882.9 °C;
钾的密度为0.856g/cm?,熔点为63.65?°C,沸点774?°C;
铷的密度为1.532g/cm?,熔点为38.89°C,沸点688°C;
铯的的密度为1.8785g/cm?,熔点为28.84?°C,沸点678.4?°C;
钫的密度为1.870g/cm?,熔点为27°C,沸点677?°C。
碱金属均有一个属于s轨道的最外层电子,因此这一族属于元素周期表的s区。碱金属的化学性质显示出十分明显的同族元素相似性,是化学元素周期性的例证之一。尽管氢也同属于第1族,但其显现的化学性质和碱金属相差甚远,因此通常不被认为是碱金属。
扩展资料:
碱金属有很多相似的性质;都是银白色的金属、密度小、熔点和沸点都比较低、标准状况下有很高的反应活性。它们易失去价电子形成带一个单位正电荷的阳离子。
它们一般质地较为柔软,可以用刀切开,露出银白色的剖面;由于能和空气中的氧气反应,剖面暴露于空气中将很快失去光泽。由于碱金属化学性质都很活泼,贮存时一般将它们放在矿物油中,或封于稀有气体中保存,以防止其与空气或水发生反应。
]在自然界中,碱金属元素只有化合态,不能以稳定单质形式存在。碱金属都能和水发生激烈的反应,生成碱性的氢氧化物,其反应能力与剧烈程度随着原子序数的增大而越强。
所有已发现的碱金属均天然存在于自然界中。按照化学元素丰度顺序,自然界化学丰度最高的是钠,其次是钾,接下来是锂、铷、铯,最后是钫。
钫的放射性很强,因此只能作为天然衰变链的产物,在自然界中痕量存在。已有实验试图合成可能的第七个碱金属Uue,但截至目前均以失败告终。
此外,由于相对论效应会极大影响包括Uue在内的超重元素的性质,因此Uue可能不是碱金属;即使它真的是碱金属,它的物理性质和化学性质也可能会和其它六个碱金属有较大差异。
碱金属有多种用途。铷或铯的原子钟是游离态碱金属元素最著名的应用实例之一,其中以铯原子钟最为精准。
钠化合物较为常见的一种用途是制作钠灯,一种高效光源。人类对食盐(氯化钠)的使用可追溯到古代。钠和钾是生物体中的电解质,具有重要的生物学功能,属于膳食矿物质。尽管其它碱金属并非膳食矿物质,它们同样会对身体产生或有益或有害的影响。
百度百科——碱金属
碱金属的硬度,密度,熔点,状态,颜色,化学性质各是啥?!急急急~~~~
金属的熔沸点主要取决于其中的金属键强度。与密度没有关系!
金属阳离子的电荷越高,半径越小,则金属键的强度越大。
LI,Na,K,Rb,Cs为同主族元素,原子半径依次增大,电荷相同。因此,随着半径的增大,金属键依次减弱,所以熔沸点逐渐降低。
碱金属的物理性质
碱金属(alkali metal)指的是元素周期表ⅠA族元素中所有的金属元素,目前共计锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr)六种,前五种存在于自然界,钫只能由核反应产生。碱金属是金属性很强的元素,其单质也是典型的金属,表现出较强的导电、导热性。碱金属的单质反应活性高,在自然状态下只以盐类存在,钾、钠是海洋中的常量元素,在生物体中也有重要作用;其余的则属于轻稀有金属元素,在地壳中的含量十分稀少
碱金属是指在元素周期表中属于第IA族的六个金属元素。 碱金属除铯以外都是银白色的(Cs略带金色光泽),质软的,化学性质活泼的金属,密度小,熔点和沸点都比较低。他们生成化合物的几乎都是正一价阳离子(在碱化物中,碱金属会以负一价阴离子的方式出现)。碱金属原子失去电子变为离子时最外层一般是8个电子,但锂离子最外层只有2个电子。电子构型通式为ns1。 因为碱金属最外层只有1个电子,所以碱金属都能和水发生激烈的反应,生成强碱性的氢氧化物,并随相对原子质量增大反应能力越强。在氢气中,碱金属都生成白色粉末状的氢化物。碱金属都可在氯气中燃烧。由于碱金属化学性质都很活泼,为了防止与空气中的水发生反应,一般将他们放在煤油或石蜡中保存。 氢虽然是第1族元素,但它在普通状况下是双原子气体,不会呈金属状态,也不属于碱金属。只有在极端情况下(1.4兆大气压力),电子可在不同氢原子之间流动,变成金属氢。有些在液氨中会形成电子盐。
地壳
下表为碱金属元素在地壳中(不含海洋、大气)的质量克拉克值,取自《无机化学(第五版)》,2008[1].371 元素 锂 钠 钾 铷 铯
w(%) 0.006% 2.64% 2.60% 0.03% 0.0006%
由表可见,碱金属中,钾、钠的丰度较大,为常量元素,锂、铷、铯丰度很小,为微量元素。而海水中,钠的质量克拉克为1.062%,钾的质量克拉克为0.038%,钾、钠同样是海水中的常量元素。[2] 矿物学 碱金属在自然界的矿物是多种多样的,常见的如下 ·锂:锂辉石、锂云母、透锂长石 ·钠:氯化钠、碳酸钠、硝酸钠、芒硝 ·钾:光卤石、氯化钾、钾长石 ·铷:红云母、铷铯矿 ·铯:铷铯矿、铯榴石
人体
碱金属在人体中以离子形式存在于体液中,也参与蛋白质的形成。 碱金属在人体中的质量分数(%)数据来源:《无机化学(第五版)》,2008.371 元素 锂 钠 钾 铷 铯
鲜重 极微量 0.15% 0.35% 极微量 —
注:数据可能存在较大差异,以下数据可供核对:氧65%、碳18%、氢10% 人体中元素与地壳元素丰度呈正相关,这是生物链的传递结果。动物胚胎中钾与钠的质量分数相近,有学者认为这是动物源于海生有机体的证据之一。 作用 ·锂离子:锂在人脑有特殊作用,研究表明,锂离子可以引起肾上腺素及神经末梢的胺量降低,能明显影响神经递质的量,因为锂离子具体的作用机理尚不清楚,故锂中毒也没有特效解药,但碳酸锂目前被广泛用于狂躁型抑郁症的治疗(口服:600mg~800mg╱天)。[1] ·钠离子:人体液的渗透压平衡主要通过钠离子和氯离子进行调节,钠离子的另一个重要作用是调节神经元轴突膜内外的电荷,钠离子与钾离子的浓度差变化是神经冲动传递的物质基础,世界卫生组织建议每人每日摄入(1~2)克钠盐,中国营养学会建议不要超过5克。[1] ·钾离子:钾也参与调节渗透压与轴突膜内外的电荷,人体中心脏、肝脏、脾脏等器官中钾比较富集。[1] ·铷元素:铷元素的生理作用目前还在研究中,有多种迹象表明铷与生命过程有关,疑似为微量元素。[3]
编辑本段元素性质
元素 3 Li(锂) 11Na
(钠) 19K(钾) 37Rb(铷) 55Cs(铯) 87Fr(钫)
熔点/℃ 180.5 .81 63.65 38.89 28.84 27
沸点/℃ 1347 822.9 774 688 678.4 677
熔沸点变化 降低趋势
密度(25℃)/g·cm^-3 0.534 0.1 0.856 1.532 1.8785 1.870
密度变化 升高趋势 反常
导电性 导 体 导 体 导 体 导 体 导 体 导 体
颜 色 银白色 银白色 银白色 银白色 略带** 红色
形 态 固 体 固 体 固 体 固 体 固 体 固 体
金属or非金属性 金属性 金属性 金属性 金属性 金属性 金属性
价 态 +1 +1 +1 +1 +1 +1
主要氧化物 Li2O Na2O Na2O2 K2O K2O2 复杂 复杂 复杂
氧化物对应的水化物 LiOH NaOH KOH RbOH CsOH FrOH
气态氢化物 LiH NaH KH RbH CsH FrH
气态氢化物的稳定性 不稳定 不稳定 不稳定 不稳定 不稳定 不稳定
周期律性质
主条目:元素周期律 碱金属位于ⅠA族,其周期律性质主要表现为 ·自上而下,碱金属元素的金属性逐渐增强 ·每一种碱金属元素都是同周期元素中金属性最强的元素
锂的特殊性
锂的反常性 ⅠA族的周期性十分明显,但锂还是和同族的其它碱金属元素有很大不同,这种不同主要表现在锂化合物的共价性,这是由锂的原子半径过小导致的。 锂-镁对角线规则 主条目:对角线规则 元素周期表中,碱金属锂与位于其对角线位置的碱土金属镁(Mg)存在一定的相似性,这里体现了元素周期表中局部存在的“对角线规则”。锂与镁的相似性表现在: ·单质与氧气作用生成正常氧化物 ·单质可以与氮气直接化和(和锂同族的其它碱金属单质无此性质) ·氢氧化物为中强碱,溶解度小,加热易分解 ·氟化物、碳酸盐、磷酸盐难溶于水 ·碳酸盐受热易分解 ·氯化物能溶于有机溶剂中(共价性) ·锂离子、镁离子的水合能力强 究其原因,锂-镁对角线规则可以用周期表中离子半径的变化来说明,同一周期从左到右,离子半径因有效电荷的增加而减少,同族元素自上而下离子半径因电子层数的增加而增大,锂与镁因为处于对角线处,镁正好在锂的“右下方”,其离子半径因周期的递变规律而减小,又因族的递变规律而增大,二者抵消后就出现了相似性。[3]
编辑本段单质与离子
物理性质
碱金属元素单质(左~右为锂~铯)
碱金属单质皆为具金属光泽的银白色金属,但暴露在空气中会因氧气的氧化作用生成氧化物膜使光泽度下降,呈现灰色,碱金属单质的密度小于2g·cm^-3,是典型的轻金属,锂、钠、钾能浮在水上,锂甚至能浮在煤油中;碱金属单质的晶体结构均为体心立方堆积,堆积密度小,莫氏硬度小于2,质软,导电、导热性能极佳。碱金属单质都能与汞(Hg)形成合金(汞齐)。[1]
化学性质
碱金属单质的标准电极电势很小,具有很强的反应活性,能直接与很多非金属元素形成离子化合物,与水反应生成氢气,能还原许多盐类(比如四氯化钛),除锂外,所有碱金属单质都不能和氮气直接化合。 与水反应 2Li+2H2O==2LiOH+H2(g) 2Na+2H2O==2NaOH+H2(g) 2K+2H2O==2KOH+H2(g) 与氧气反应 4Li(s)+O?(g)——→2Li2O(s) 2Na(s)+O?(g)——→Na2O?(s) M(s)+O?(g)——→M2O(s)M=K、Rb、Cs 与卤素(X)反应 2M(s)+X?(g)——→2MX(s) 与氢气(H?)反应 2M(s)+H?(g)——→2MH(s) 与硫反应 M(s)+S(s)——→M2S(s) 与磷反应 M(s)+P(s)——→M3P(s) 锂与氮气反应 6Li(s)+N2(s)——→2Li3N(s) 焰色反应 碱金属离子及其挥发性化合物在无色火焰中燃烧时会显现出独特的颜色,这可以用来鉴定碱金属离子的存在,锂、铷、铯也是这样被化学家发现的,电子跃迁可以解释焰色反应,碱金属离子的吸收光谱落在可见光区,因而出现了标志性颜色。 除了鉴定外,焰色反应还可以用于制造焰火和信号弹。 下表给出碱金属离子的焰色反应相关表格,波长数据取自《无机化学(第五版)》,2008[1]380 类别 锂离子 钠离子 钾离子 铷离子 铯离子
颜色 紫红 黄 淡紫 紫 蓝
波长/nm 670.8 589.2 766.5 780.0 455.5
热力学及电化学性质
碱金属的相关热力学及电化学数据见下 数据取自《无机化学(第五版)》,2008[1].375 电子亲和能数据取自《化学-物质结构与性质(选修)》,2007年[4].24 单位均为标准单位 类别 锂 钠 钾 铷 铯
标准摩尔升华焓 159.37 107.32 89.24 80.88 76.065
标准摩尔水合焓 -535.27 -420.48 -337.64 -312.27 -287.24
离子标准摩尔生成焓(aq) 150.51 188.88 176.62 177.83 170.72
第一电离能(I) 526.41 502.04 425.02 409.22 381.90
电子亲和能(E) 59.6 52.9 48.4 46.9 45.5
标准电极电势E⊕ -3.040 -2.714 -2.936 -2.943 -3.027
由表中可以看出碱金属的标准电极电势都在-3.000V左右,表明其单质很容易失去电子,电离能不断增加,电子亲和能不断递减,表明其单质的还原性不断增强,锂的标准摩尔水合焓最大,但事实上锂与水最不易反应,这是因为锂的标准摩尔升华焓太大,且锂与水的反应产物氢氧化锂不溶于水,覆盖在锂上,影响了反应。[1]
编辑本段化合物
在碱金属元素形成的各类化合物中,碱金属阳离子是没有特别性质的,碱金属化合物的性质在绝大多数情况现为阴离子的性质。
氧化物
碱金属单质与氧气能生成各种复杂的氧化物 正常氧化物 碱金属中,只有锂可以直接生成氧化物,其它碱金属单质的氧化物可以被继续氧化 4Li(s)+O?(g)——→2Li2O(s) 碱金属的正常氧化物是反磁性物质,都能与水反应生成对应的氢氧化物 M2O(s)+H2O(l)——→MOH(aq) 碱金属正常氧化物的相关性质见下,取自《无机化学(第五版)》,2008[1].383 单位均为标准热力学单位 类别 氧化锂 氧化钠 氧化钾 氧化铷 氧化铯
颜色 白 白 淡黄 亮黄 橙红
熔点/K 1743.15 1093.15 ~523.15(分解) ~573.15(分解) ~663.15(分解)
标准摩尔生成焓 -5.9 -414.22 -361.5 -339 -345.77
过氧化物 所有碱金属都能形成过氧化物,除锂外,其它碱金属可以直接化合得到过氧化物,碱金属的过氧化物呈淡** 2M(s)+O?(g)——→M2O?(s) 过氧化物中的氧元素以过氧阴离子的形式存在,过氧根离子的键级为1。过氧化物是强碱(质子碱),能与水反应生成碱性更弱的氢氧化物和过氧化氢,由于反应大量放热,生成的过氧化氢会迅速分解产生氧气。 2M2O?(s)+2H2O(l)——→4MOH(aq)+H2O?(aq) 2H2O?(aq)——→2H2O(l)+O?(g) 过氧化物可与酸性氧化物反应生成对应的正盐,若与之反应的酸性氧化物有较强还原性,则有被氧化的可能 M2O?(s)+2CO?(g)——→2M2CO?(s)+O?(g) M2O?(s)+2SO?(g)——→2M2SO?(s) 过氧化物在熔融状态下可与某些铂系元素形成含氧酸盐 Ru(s)+3M2O?(l)——→M2RuO?(s)+2M2O(l) 过氧化物中常见的是过氧化钠(Na2O?)和过氧化钾(K2O?),它们可用于漂白,熔矿,生氧。 超氧化物 除锂外,所有碱金属元素都有对应的超氧化物,钾、铷、铯能在空气中直接化和得到超氧化物,超氧化钾为淡黄~橙**,超氧化铷为棕色,超氧化铯为深**。 M(s)+O?(g)——→MO?(s) 超氧化物中存在超氧离子,分子轨道表明超氧离子存在一个σ键和一个3电子π键,键级为3/2,有顺磁性。 超氧化物能与水反应生成对应氢氧化物,氧气和过氧化氢,反应大量放热,过氧化氢分解 2MO?(s)+2H2O(l)——→2MOH(aq)+H2O?(l)+O?(g) 2H2O?(aq)——→2H2O(l)+O?(g) 超氧化物能与酸性氧化物反应,类似过氧化物,其中,超氧化钾与二氧化碳的反应被应用于急救空气背包中 4MO?(s)+2CO?(g)——→2M2CO?(s)+3O?(g) 超氧化钾是最为常见的超氧化物 臭氧化物 除锂外,干燥的碱金属氢氧化物固体与臭氧(O?)反应,产物在液氨中重结晶可得到臭氧化物晶体 6MOH(s)+4O?(g)——→4MO?(s)+2MOH·H2O(s)+O?(g) 臭氧化物在放置过程中缓慢分解 2MO?(s)——→2MO?(s)+O?(g) 臭氧化物中存在臭氧离子,V型结构,键级为1/3,极不稳定,具有顺磁性 臭氧化物的其他性质与超氧化物类似,不再赘述。
氢化物
碱金属单质在氢气流中加热就可获得对应的氢化物 2M(s)+H?(g)——→2MH(s) 碱金属氢化物中以氢化锂(LiH)最为稳定,850℃分解 碱金属氢化物属于离子型氢化物,熔沸点高,晶体结构为氯化钠型,碱金属氢化物中存在氢负离子,电解溶于氯化锂的氢化锂可以在阳极得到氢气,这可以证明氢负离子的存在。 碱金属氢化物与水剧烈反应放出氢气 MH(s)+H2O(l)——→MOH(aq)+H?(g)
氢氧化物
碱金属元素的氢氧化物常温下为白色固体,可溶或易溶于水,溶于水放出大量热,在空气中会发生潮解并吸收酸性气体;除氢氧化锂外其余的碱金属氢氧化物都属于强碱,在水中完全电离。 2MOH(s)+CO?(g)——→M2CO?(s)+H2O(l) 2MOH(aq)+2Al(s)+2H2O(l)——→2MAlO?(aq)+3H?(g) 2MOH(aq)+Al2O?(s)——→2MAlO?(aq)+H2O(l) 3MOH(aq)+FeCl?(aq)——→Fe(OH)?(s)+3MCl(l) 碱金属氢氧化物中以氢氧化钠和氢氧化钾最为常见,可用作干燥剂。
有机金属化合物
碱金属的有机金属化合物在有机合成上有重要应用,以下对常见物种简要介绍其中 烃(烷)基锂 烃基锂中存在桥键(LI-C-Li),以四聚体的形式存在,烃基锂中碳-锂键具有共价键的特征,其中丁基锂具有挥发性,并能进行减压蒸馏就是一个例子。[5]烃基锂是强亲核试剂,亲核能力优于格氏试剂,能引发后者的所有加成反应,并有更高的产率,但立体选择性差;烃基锂位阻小,反应时受空间效应的影响小,因此可用烃基锂合成位阻较大的醇,此外,烃基锂与铜(Ⅰ)卤化物可形成二烃基铜锂,在有机合成上也有重要应用。烃基锂容易与水反应,制备时要彻底干燥。[6] 炔基钠 1-炔烃可与钠在液氨中生成炔基钠,炔基钠是亲核试剂,可与卤代烃反应备制炔的衍生物或增长碳链,此外,也可以与酰卤反应备制炔基酮,但在有机合成中应用较少,其替代品为炔基铜(Ⅰ)化合物。[6]
络合物
冠醚络合物 冠醚的中央存在一个特定大小的空腔,可与碱金属离子络合形成络合物,常见的有 锂离子:12-冠-4 钠离子:15-冠-5 钾离子:18-冠-6 钾离子与[2.2.2]穴醚形成的络合物
穴醚络合物 碱金属离子也可与穴醚络合,生成的络合物比冠醚络合物稳定,常见的有 钾离子:[2.2.2]穴醚 应用 ·表面活性剂(surfactant) ·相转移催化剂(Phase transfer catatysis PTC) ·分离对应的碱金属离子
盐
碱金属的盐类大多为离子晶体,而且大部分可溶于水,其中不溶的盐类有 ·锂盐:氟化锂、碳酸锂、磷酸锂[1] ·钠盐:六亚硝酸合钴(Ⅲ)酸钠钾、醋酸铀酰钠、六羟基合锡(Ⅳ)酸钠[1]、三钛酸钠、铋酸钠 ·钾盐:六亚硝酸合钴(Ⅲ)酸钠钾、高氯酸钾、四苯基硼(Ⅲ)酸钾[1] 碱金属的盐类熔沸点较高,下表即为碱金属盐类的熔点,本表取自《无机化学(第五版)》,2008[1].387 单位:m.p./℃
锂 钠 钾 铷 铯
氯化物 613 801 771 715 646
硫酸盐 859 880 1069 1050 1005
硝酸盐 ~225 307 333 305 414
碳酸盐 720 858 901 837 792
从表中还可以观察到:锂盐的沸点明显偏低,表明锂盐表现出一定的共价性 卤化物 碱金属卤化物中常见的是氯化钠和氯化钾,它们大量存在于海水中,电解饱和氯化钠可以得到氯气,氢气和氢氧化钠,这是工业制取氢氧化钠和氯气的方法。 阳极:2Cl--2e- ——→Cl?↑ 阴极:2H++2e- ——→H?↑ 总反应:2NaCl+2H2O——→2NaOH+H?↑+Cl?↑ 硫酸盐 碱金属硫酸盐中以硫酸钠最为常见,十水合硫酸钠俗称芒硝,用于相变储热,无水硫酸钠俗称元明粉,用于玻璃、陶瓷工业及制取其它盐类。[1] 硝酸盐 碱金属的硝酸盐在加强热时分解为亚硝酸盐 2MNO?(s)——→2MNO?(s)+O?(g) 硝酸钾(KNO?)和硝酸钠(NaNO?)是常见的硝酸盐,可用作氧化剂 碳酸盐 碱金属的碳酸盐中,碳酸锂可由含锂矿物与碳酸钠反应得到,是制取其它锂盐的原料,还可用于狂躁型抑郁症的治疗;碳酸钠俗名纯碱,是重要的工业原料,主要由侯氏制碱法生产。[1] NH?(g)+H2O(l)+CO?(g)——→NH4HCO?(aq) NH4HCO?(aq)+NaCl(s)——→NH4Cl(aq)+NaHCO?(s) 2NaHCO?(s)—△→Na2CO?(s)+H2O(l)+CO?↑(g)
1.相似性:(1)银白色(铯略带金色) (2)硬度小 (3)密度小
(4)熔点低(5)导热、导电
2.递变规律:从锂到铯
(1)密度呈减小趋势(但钾反常)
(2)熔点、沸点逐渐降低
一般地说,随着原子序数的增加,单质的密度增大。但从Na到K出现了“反常”现象,根据密度公式ρ=m/V,Na到K的相对原子质量增大所起的作用小于原子体积增大所起的作用,因此K的密度比钠的密度小。
金**金属,性软而轻,具有延展性。密度1.8785克/厘米3。熔点28.40±0.01℃,沸点678.4℃。
1公斤的高纯金属铯化合价+1。电离能3.894电子伏特。在碱金属中它是最活泼的,能和氧发生剧烈反应,生成多种氧化物(据《元素化学》介绍至少有7种)的混合物。在空气中,氧化的热量足以使铯熔化并点燃。氯化铯、碳酸铯是它的主要化合物
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。












