金属单质和非金属单质反应生成盐_金属单质加非金属单质生成盐的例子
1.氧化还原反应有哪些
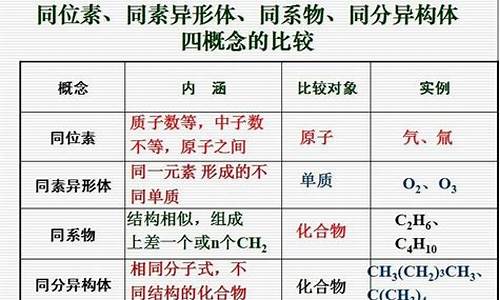
1、金属+非金属→盐: 活泼或比较活泼的金属与非金属在点燃或加热条件下发生反应,生成无氧酸盐(氧气与金属反应生成氧化物)。例如:2Na +Cl2==点燃==2NaCl、Fe+S==加热==FeS。
2、金属+酸→盐+氢气:在金属活动性顺序表中排在H前面的金属,与稀酸反应可以生成盐,如:Fe+H2SO4==FeSO4+H2↑2Na +2HCl==2NaCl +H2↑。活泼金属K、Ca、Na因反应太剧烈,不易控制,不宜直接与酸反应制取盐;酸不能用硝酸或浓硫酸以及不溶性酸(如硅酸)和很弱的酸(如碳酸);若生成的盐是难溶,则会覆盖在金属表面影响反应的继续进行,如铅蓄电池放电时的阴极反应Pb+H2SO4==PbSO4↓+H2↑
3、金属+盐→新金属+新盐:在金属活动性顺序表中排在前面的金属,可把后面的金属从它的盐溶液中置换出来,如湿法炼铜反应Fe+CuSO4==FeSO4+Cu活泼金属(K、Ca、Na)不能置换出盐溶液中的金属,如把Na放入硫酸铜溶液中,发生的反应是:2Na+CuCl2+2H2O==2NaCl+Cu(OH)2↓+H2↑
4、碱性氧化物+酸性氧化物→盐: 如CaO+CO2==CaCO3
5、碱性氧化物+酸→盐+水:不溶性碱性氧化物与强酸才能发生反应生成盐和水,如用稀盐酸(或稀硫酸)除铁锈反应6HCl+Fe2O3==2FeCl3+3H2O 。
6、酸性氧化物+碱→盐+水:要求碱是可溶或微溶,如工业上用石灰浆或氢氧化钠来吸收含二氧化硫的废气SO2+Ca(OH)2==CaSO3↓+H2O。
7、酸+碱→盐+水:酸和碱两者必须有一种是强酸或强碱,如Mg(OH)2+H2SO4==MgSO4+2H2O“双弱”不能反应,如碳酸与氢氧化铁、氢氧化锌等不会反应。
8、碱+盐→新碱+新盐:参加反应的碱和盐都要可溶,反应的新碱或新盐至少有一种是不溶,如3NaOH +FeCl3==3 NaCl + Fe(OH)3↓
9、酸+盐→新酸+新盐:要求生成的盐是难溶或生成的酸是挥发性的酸或不稳定的酸,如CaCO3 +2HCl==2CaCl2+CO2↑+H2O如果反应的盐是不溶的,则生成的盐要求可溶,否则生成的难溶盐会覆盖在反应物表面使反应不能继续进行,实验室用石灰石制取二氧化碳用盐酸而不能用硫酸就是这个原因。AgCl 和BaSO4等既不溶于水,又不溶于酸,也不与酸发生反应物质,不能生成新盐。
10、盐+盐→新盐+新盐:参加反应的两种盐必须都可溶,生成物至少有一种是沉淀。如Na2CO3+BaCl2== 2NaCl+BaCO3↓。
氧化还原反应有哪些
2、盐
盐
碱
酸
盐
碱
碱
3、HCl
H2SO4
HNO3
H2CO3
H2SO3
H3PO4
4、NaOH
Ca(OH)2
Cu(OH)2
Fe(OH)3
Ba(OH)2
Mg(OH)2
Al(OH)3
Zn(OH)2
KOH
3、(1)气体单质:H2
O2
固体单质:C
Na
非金属氧化物:H2O
CO2
金属氧化物:Na2O
酸:H2CO3
碱NaOH
盐:NaHCO3
Na2CO3
(2)空气最多:N2
复燃:O2
非金属氧化物:H2O
NO
NO2
N2O3
N2O5
N2O
酸:HNO3
HNO2
碱NH4OH
盐NH4NO3。
二、依次
红
蓝
紫
蓝
蓝
红
无
红
无
红
红
无
<
>
=
>
>
<
三、NaOH√
CuSO4√
KNO3√
CaCO3╳
BaSO4╳
AgNO3√
Cu(OH)2
╳FeCl3
√BaCO3╳
Na2SO4√
Na2CO3√
MgCl2√
KCl√
Ca(OH)2√
Al2(SO4)3
√ZnSO4
√FeSO4√
CuSO4√
AgCl╳
关于氧化还原反应的具体内容如下:
1、金属与非金属的反应:这类反应通常是金属单质与非金属单质发生化合反应,生成金属非金属化合物。在这个过程中,金属元素失去电子被氧化,非金属元素获得电子被还原。例如:2Na+Cl2→2NaCl(钠与氯气反应生成氯化钠)。
2、金属与酸的反应:这类反应通常是金属单质与酸发生置换反应,生成盐和氢气。在这个过程中,金属元素失去电子被氧化,氢离子获得电子被还原。例如:Fe+2HCl→FeCl2+H2(铁与盐酸反应生成氯化亚铁和氢气)。
3、非金属与碱的反应:这类反应通常是非金属单质与碱发生置换反应,生成盐和水。在这个过程中,非金属元素获得电子被还原,氢氧根离子失去电子被氧化。例如:Cl2+2NaOH→NaCl+NaClO+H2O(氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水)。
4、氧化剂与还原剂的反应:这类反应通常是氧化剂与还原剂发生化合反应,生成氧化物和还原物。在这个过程中,氧化剂获得电子被还原,还原剂失去电子被氧化。例如:2KClO3→2KCl+3O2(氯酸钾分解生成氯化钾和氧气)。
5、燃烧反应:燃烧是一种典型的氧化还原反应,燃料中的碳、氢等元素与氧气发生化合反应,生成二氧化碳、水等物质。在这个过程中,燃料中的碳、氢等元素失去电子被氧化,氧气获得电子被还原。
氧化还原反应在日常生活和工业生产的应用如下:
1、燃烧:燃烧是一种典型的氧化还原反应,燃料中的碳、氢等元素与氧气发生化合反应,生成二氧化碳、水等物质。燃烧反应为人类提供了能源,如煤、石油、天然气等化石燃料的燃烧产生大量的热能,用于发电、供暖、烹饪等。
2、金属的防腐:许多金属在潮湿的环境中容易发生腐蚀,导致金属的损耗。通过在金属表面涂覆一层防腐剂,可以减缓金属的腐蚀速度。防腐剂通常是具有还原性的化合物,如锌、铝等,它们在金属表面形成一层保护膜,阻止金属与氧气、水分等发生氧化还原反应。
3、电化学:电化学是研究电能与化学能之间相互转化的科学。许多电化学过程都涉及到氧化还原反应,如电镀、腐蚀、电池等。例如,在电解过程中,电解质溶液中的离子在电极上发生氧化还原反应,产生电流。
4、生物体内的代谢:生物体内的许多生理过程都涉及到氧化还原反应。例如,呼吸作用是生物体获取能量的过程,其中的氧化还原反应将葡萄糖等有机物分解为二氧化碳和水,同时释放出能量。
5、工业生产:许多工业生产过程中都涉及到氧化还原反应。例如,化肥生产过程中的氨合成、硫酸生产中的二氧化硫氧化等都是典型的氧化还原反应。此外,许多化工产品(如染料、药品、塑料等)的生产过程中也涉及到氧化还原反应。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。